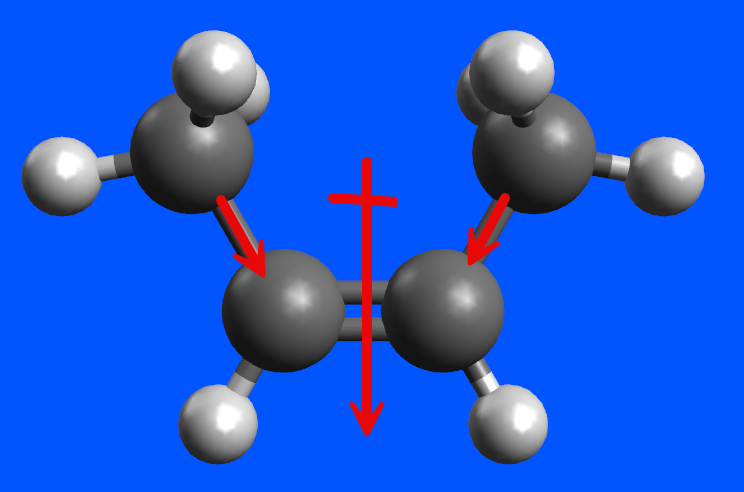
So sánh tính chất vật lí của cis/trans-alkene
1. GIỚI THIỆU
Alkene là hydrocarbon chứa ít nhất một liên kết đôi carbon-carbon (C = C). Không giống như liên kết đơn, liên kết đôi C=C hạn chế quay, giúp tạo một loại đồng phân lập thể đặc biệt được gọi là đồng phân hình học (hoặc đồng phân cis-trans). Khi hai nhóm thế khác nhau được gắn vào mỗi carbon liên kết đôi, có thể có hai sự sắp xếp không gian riêng biệt: dạng cis (cùng bên) và dạng trans (trái bên). Mặc dù đồng phân cis và trans có cùng công thức phân tử và kết nối, nhưng chúng khác nhau đáng kể về tính chất vật lý do sự khác biệt về hình học phân tử, kiểu đối xứng và sự phân cực.
Cặp cis-but-2-ene và trans-but-2-ene (công thức phân tử C₄H₈) là một trong những ví dụ được nghiên cứu nhiều nhất và đóng vai trò là một mô hình rất tốt để hiểu rõ về những khác biệt này.
2. TỔNG QUAN VỀ CẤU TRÚC
2.1 cis-but-2-ene
Trong cis-but-2-ene, cả hai nhóm methyl (–CH₃) đều ở cùng một phía của liên kết đôi. Sự sắp xếp này tạo ra sự phân bố điện tích không đối xứng trên phân tử, dẫn đến xuất hiện moment lưỡng cực.
2.2 trans-but-2-ene
Trong trans-but-2-ene, hai nhóm methyl nằm ở hai phía đối diện của liên kết đôi. Sự sắp xếp này tạo cho phân tử một trung tâm đối xứng, làm cho các lưỡng cực liên kết riêng lẻ triệt tiêu lẫn nhau, dẫn đến moment lưỡng cực bằng không.
3. SO SÁNH CÁC TÍNH CHẤT VẬT LÍ CHÍNH
3.1 Điểm sôi
Tính chất | cis-But-2-ene | trans-But-2-ene |
Điểm sôi | 3,7 °C | 0,9 °C |
cis-But-2-ene có nhiệt độ sôi cao hơn so với đồng phân trans của nó. Lý do ở sự phân cực:
- Đồng phân cis có moment lưỡng cực (≈ 0,33 D), vì vậy ngoài lực phân tán London (một trong các dạng tương tác van der Waals), nó còn có tương tác lưỡng cực-lưỡng cực giữa các phân tử. Những lực hấp dẫn liên phân tử bổ sung này đòi hỏi nhiều năng lượng hơn để có thể tách riêng các phân tử, làm tăng điểm sôi.
- Đồng phân trans không phân cực (moment lưỡng cực ≈ 0 D) và chỉ dựa vào lực phân tán London, yếu hơn đối với các phân tử có kích thước và hình dạng tương đương, dẫn đến nhiệt độ sôi thấp hơn.
3.2 Điểm nóng chảy
Tính chất | cis-But-2-ene | trans-But-2-ene |
Điểm nóng chảy | −138,9 °C | −105,5 °C |
Ở đây tình hình bị đảo ngược: trans-but-2-ene có nhiệt độ nóng chảy cao hơn cis-but-2-ene. Điều này là do đồng phân trans có hình dạng gần như thẳng hàng, đối xứng hơn, cho phép các phân tử đóng gói với nhau hiệu quả hơn trong mạng tinh thể rắn. Đóng gói tốt hơn làm tăng năng lượng mạng tinh thể và do đó cần nhiều nhiệt năng hơn để nóng chảy. Đồng phân cis, bị uốn cong hoặc “gấp khúc”, đóng gói kém hiệu quả hơn, dẫn đến lực tinh thể yếu hơn và nhiệt độ nóng chảy thấp hơn.
Sự đảo ngược này – điểm sôi cao hơn đối với cis, điểm nóng chảy cao hơn đối với trans – là một xu hướng chung được quan sát thấy trên nhiều cặp đồng phân hình học.
3.3 Moment lưỡng cực
Tính chất | cis-But-2-ene | trans-But-2-ene |
Moment lưỡng cực | ≈ 0,33 D | ≈ 0 D |
Đây là nguyên nhân gốc rễ của hầu hết các khác biệt khác. Đồng phân cis phân cực; đồng phân trans không phân cực. Phân cực phát sinh do các lưỡng cực liên kết C–CH₃ ở dạng cis chỉ theo cùng một hướng chung, tạo ra một lưỡng cực kết quả. Ở dạng trans, chúng chỉ theo các hướng ngược nhau và hủy bỏ.
3.4 Mật độ
Đồng phân cis thường đặc hơn một chút so với đồng phân trans trong pha lỏng do tương tác giữa các phân tử mạnh hơn kéo các phân tử lại gần nhau hơn một chút, mặc dù sự khác biệt là rất nhỏ (cả hai đều xấp xỉ 0,62 g / cm³ tại điểm sôi tương ứng của chúng).
3.5 Độ ổn định và enthalpy của quá trình đốt cháy
Đồng phân trans ổn định nhiệt động lực học hơn một chút so với đồng phân cis. Điều này có thể được giải thích bởi biến dạng lập thể: ở dạng cis, hai nhóm methyl ở cùng một phía và chịu lực đẩy không gian lớn hơn, làm tăng năng lượng bên trong của phân tử. Nhiệt độ hydrogen hóa xác nhận điều này:
Tính chất | cis-But-2-ene | trans-But-2-ene |
Hydrogen hóa ΔH ° (kJ / mol) | −119,7 · | −115,5 · |
Đồng phân cis giải phóng nhiều năng lượng hơn khi hydrogen hóa, cho thấy nó ở trạng thái năng lượng cao hơn – tức là kém ổn định hơn – so với đồng phân trans.
3.6 Độ hòa tan
Cả hai đồng phân về cơ bản không hòa tan trong nước và có thể trộn lẫn với dung môi hữu cơ không phân cực, vì cả hai đều chủ yếu là hydrocarbon không phân cực. Tuy nhiên, cis-alkene có moment lưỡng cực đáng kể có thể cho thấy khả năng hòa tan lớn hơn một chút trong dung môi phân cực so với các đồng phân trans của chúng – một sự khác biệt trở nên rõ rệt hơn trong các hệ thống alkene mạch dài hơn.
4. BẢNG TÓM TẮT
Tính chất vật lý | cis-But-2-ene | trans-But-2-ene | Giải thích |
Điểm sôi | 3,7 °C | 0,9 °C | Lực lưỡng cực-lưỡng cực trong cis làm tăng điểm sôi |
Điểm nóng chảy | −138,9 °C | −105,5 °C | Đóng gói tinh thể tốt hơn của trans tăng điểm nóng chảy |
Moment lưỡng cực | ≈ 0,33 D | ≈ 0 D | Lưỡng cực liên kết trái chiều và triệt tiêu lẫn nhau trong trans (đối xứng) |
Ổn định nhiệt động lực học | Thấp hơn | Cao hơn | Sức căng lập thể lớn hơn trong cis (hai nhóm methyl cùng bên) |
Hydrogen hóa ΔH ° (kJ / mol) | −119,7 | −115,5 | Cis có năng lượng ở trạng thái cơ bản cao hơn |
Độ hòa tan trong nước | Rất thấp | Rất thấp | Cả hai đều chủ yếu là hydrocarbon không phân cực |
5. XU HƯỚNG CHUNG (từ but-2-ene)
Các mô hình quan sát được đối với but-2-ene cũng khái quát hóa các cặp cis/trans alkene khác:
- Điểm sôi: các đồng phân cis hầu như luôn sôi ở nhiệt độ cao hơn các đồng phân trans tương ứng có cùng mạch carbon, do các tương tác lưỡng cực – lưỡng cực bổ sung đã nêu trên.
- Điểm nóng chảy: các đồng phân trans hầu như luôn nóng chảy ở nhiệt độ cao hơn, vì hình dạng của chúng cho phép đóng gói tinh thể hiệu quả hơn.
- Tính ổn định: các đồng phân trans thường ổn định hơn về mặt nhiệt động lực học do giảm lực đẩy lập thể giữa các nhóm thế cồng kềnh.
Những xu hướng này rất quan trọng trong công nghiệp hóa học (ví dụ, trong tổng hợp xúc tác các đồng phân alkene cụ thể để sản xuất polymer) và trong hóa sinh, trong đó các liên kết đôi cis trong acid béo không bão hòa chịu trách nhiệm cho cấu trúc gấp khúc giữ cho màng tế bào luôn linh hoạt.
6. TÀI LIỆU THAM KHẢO
- Clayden, J., Greeves, N., & Warren, S. (2012). Organic Chemistry (2nd ed.). Oxford University Press. pp. 105–115.
- McMurry, J. (2015). Organic Chemistry (9th ed.). Cengage Learning. pp. 164–172.
- Atkins, P., & de Paula, J. (2014). Physical Chemistry (10th ed.). Oxford University Press. pp. 638–641.
- Silverstein, R. M., Webster, F. X., & Kiemle, D. J. (2014). Spectrometric Identification of Organic Compounds (8th ed.). John Wiley & Sons.
- NIST WebBook — Thermophysical Properties of But-2-ene isomers. National Institute of Standards and Technology. Retrieved from https://webbook.nist.gov/
- Eliel, E. L., & Wilen, S. H. (1994). Stereochemistry of Organic Compounds. John Wiley & Sons. pp. 9–50.